该研究是GSK公司研发的一种诱导性T细胞共刺激因子(ICOS)激动剂GSK3359609单药或者联合帕博利珠单抗在多瘤种中的尝试。
2019年ESMO年会上公布了INDUCE-1研究在头颈部鳞癌(HNSCC)扩展组的数据。这部分HNSCC患者先前接受过≤5种系统性治疗。单药组均接受过PD-1/L1疗法,GSK3359609治疗剂量为1mg/kg。联合治疗队列患者,接受0.3mg/kg剂量GSK3359609和200mg剂量帕博利珠单抗。
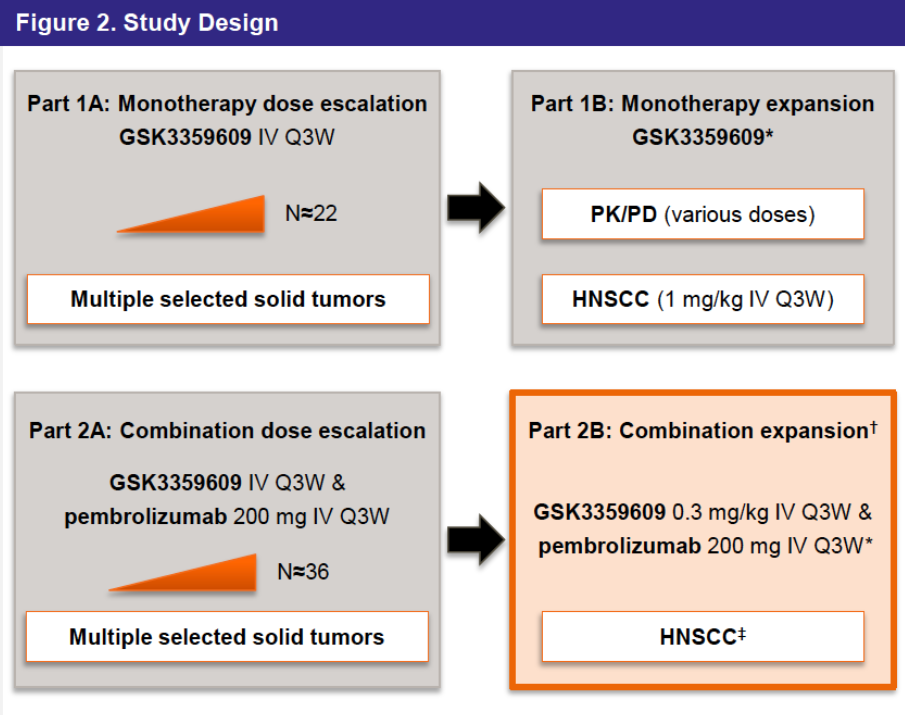
图1. INDUCE-1研究设计[2]
结果显示,联合组的34例可评估患者中,总缓解率(ORR)为24%(n=8,95%CI:11~58.7);所有应答患者缓解持续时间≥6个月(中位时间未达到;95%CI:4.2个月~NR);中位无进展生存期(PFS)为5.6个月(95%CI:2.4~7.4)。单药在在16例可评估患者中,总缓解率(ORR)为6%(n=1,95%CI:0.2~30.2)。
ICOS在黑色素瘤中高度表达,是抗CTLA-4治疗反应的生物标志物,临床前模型中证实了ICOS激动剂与ICIs联合可起到协同增效。INDUCE-1研究的初步数据(剂量递增阶段)也显示免疫检查点抑制剂(ICIs)在既往失败或者耐药的黑色素瘤患者治疗中有效。本研究公布了INDUCE-1研究黑色素瘤扩展组的数据(图1,类似于Part 1B和2B单药或联合用药的扩展阶段)。
跟前面的头颈部肿瘤相似(图1),入组条件:ICIs耐药或者复发的晚期黑色素瘤(除外葡萄膜黑色素瘤),先前接受过≤5种系统性治疗,之前接受抗PD-1/L1治疗达到缓解或稳定,之前没有≥3级irAE导致停药。在单药组和联合组中,被随机分为0.3或1mg/kg;每3周给予治疗35个周期,直到疾病进展或不可接受的毒性。评价其安全性和有效性。分析肿瘤活检中的生物标志。
截止到2020年3月30日,单药组种有39例可评价(0.3mg/kg组21例;1 mg/kg组18例);所有患者既往均为PD-1/L1单抗失败的;21/39(54%)为CTLA-4单抗失败的;7/39(18%)≥4种系统治疗。总体有效率为10%(4/39;1例完全缓解,3例部分缓解);疗效持续时间(DoR)为2.0+至6.3个月。BRAF和NRAS状态与否不影响疗效。使用过CTLA-4单抗的有效率明显高于未使用过CTLA-4单抗的患者。
在联合组的17例患者中,所有患者均为PD-1单抗耐药的,12/17(71%)例为抗CTLA-4耐药的;15/17(88%)例因进展停止治疗。总体有效率为18%(3/17),DoR为7.9±8.2个月,疾病控制率为53%(9/17),1例SD患者肿瘤缩小10%。
正在进行的单药扩展组分析显示,在ICOS高表达的患者中,有效率为28.6%(2/7),DoR为2.0±6.3个月,mOS为~26个月。
这是第一个在ICIs复发难治的黑色素瘤中具有单剂活性的ICOS激动剂,联合PD-1单抗治疗具有良好的临床疗效和安全性。
在过去15年中,靶向ICOS、GITR、OX40、CD27和4-1BB等共刺激受体的激动剂抗体在早期试验中始终未能达到较高的期望。可能原因在于用抗体增强T淋巴细胞的活性信号时,可能过度刺激导致其耗竭或死亡。
ICOS与其它共刺激受体不同。它与CD28同属一个家族(其余均为TNF受体家族),但其共刺激作用比CD28温和,且仅在T细胞激活后才可诱导,但在某些瘤内Treg细胞上的表达高于效应T细胞。某些公司开发的ICOS激动剂,如KY1044(IgG1抗体)被开发用来耗尽肿瘤微环境中的Treg细胞。GSK公司的ICOS激动剂(IgG4抗体)以“非耗竭T细胞”(消除ADCC)来发挥作用。
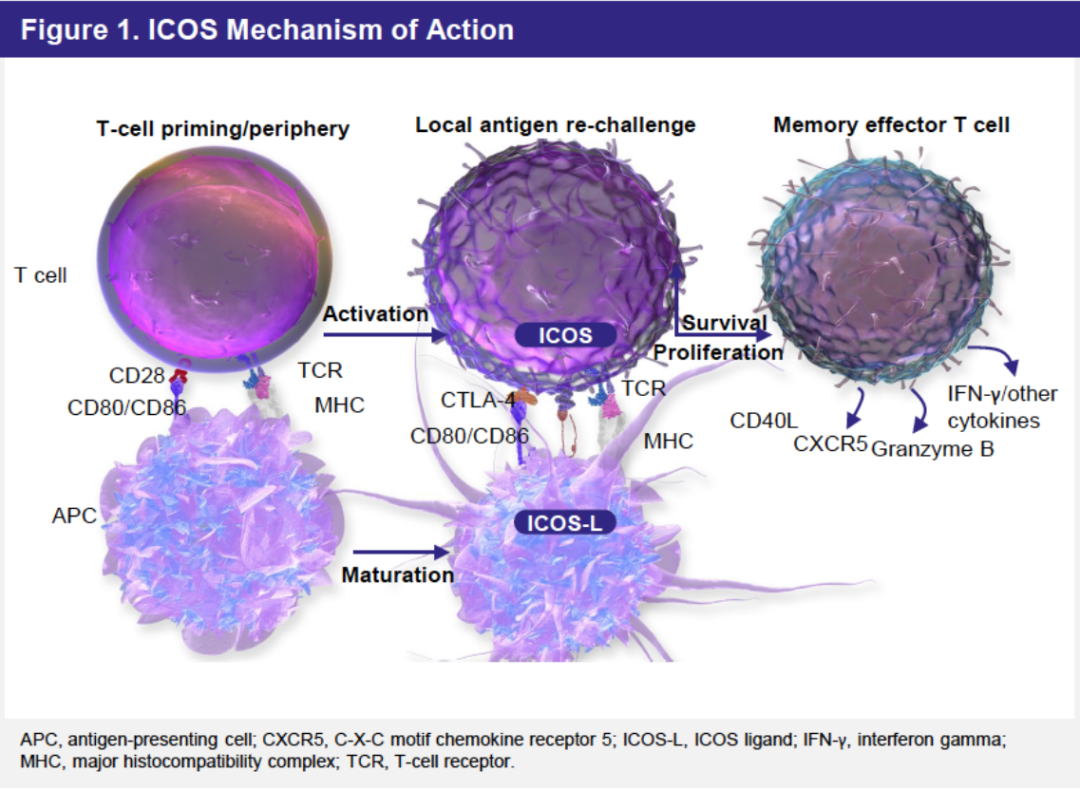
图2. ICOS的作用机制示意图[2]
共刺激受体活化剂与PD-1单抗的联合在理论上来说是可行的,但是存在很多问题,譬如:
1、联合顺序
很多联合治疗是同时给药,但可能会导致两种抗体的作用会被抵消。这在2017年的两个研究中都被证实,如果先后给药(如先使用OX40激动剂,后使用PD-1抑制剂)则能促进抗肿瘤活性,这似乎与“实际开车”的情况正好相反。
2、改进药物研发
尽管临床前研究已经充分验证了针对OX40、4-1BB、GITR、CD27、ICOS靶点的激动型抗体的活性,特别是与PD-1/L1免疫检查点抑制剂联用的抗肿瘤效果令人鼓舞,但是早期临床研究结果并不尽如人意。激动剂抗体能否发挥出最优效果,取决于多种因素,包括抗体亲和力、结合表位、交联活性、激动活性、是否阻断内源受体与配体的结合等,有赖于进一步推动药物研发。





 京公网安备 11010502033352号
京公网安备 11010502033352号